
日新製薬が製造販売する医薬品に用いる原薬の供給業者は、以下のようにして選定しています。
原薬供給業者(製造所、国内管理人)選定の流れ
原薬の製造所は国内であれば問題ないということではありません。また、ジェネリック医薬品は薬価が安いからといって、安価で品質の悪い原薬を使用することはありません。日新製薬では、国内外問わず、品質、供給体制、コストバランス、製造キャパシティー等様々な評価を行い、高品質で安定供給可能な原薬を選定しています。
▼この表は横にスクロールできます
| 1.求める原薬 要件の明確化 |
原薬要件の明確化 ・情報を収集し、規格、グレード、特許の有無、その他製剤を製造するのに必要な要件を明確にする |
|---|---|
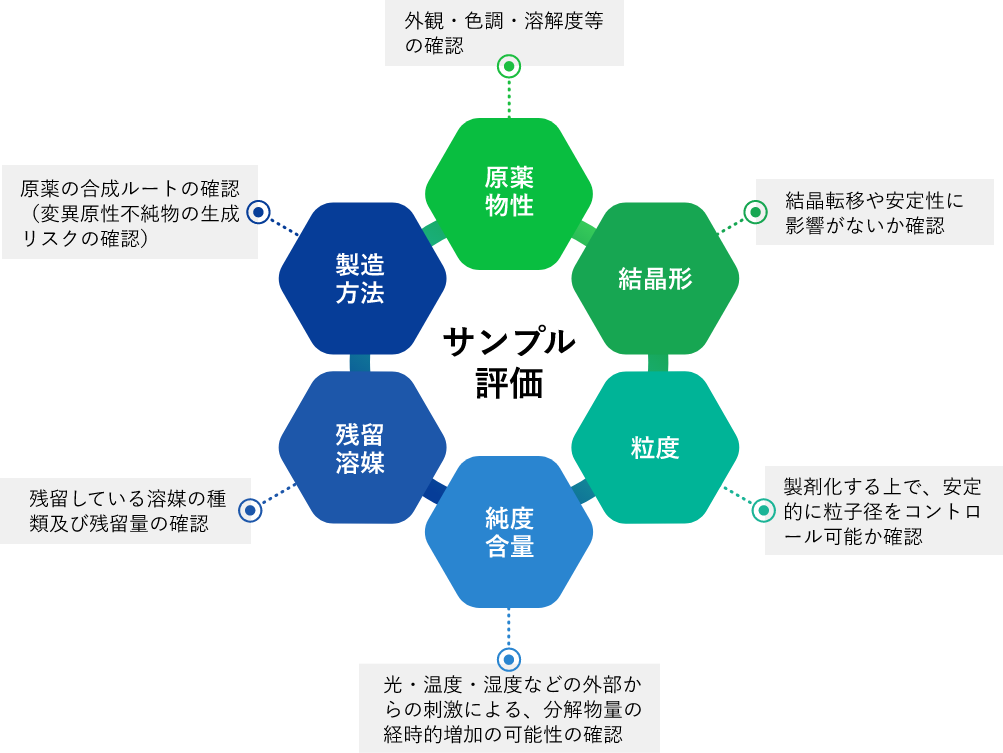
| 2.品質評価 | サンプル、試験成績書(COA)等を元に品質評価 ・物性・結晶形・粒度・純度・残留溶媒・製造方法などの評価 |
| 3.原薬供給業者 の評価と選定 |
原薬供給業者(製造所、国内管理人)の適格性評価 ・新規取引業者 → 購買要件、供給業者(国内管理人含む)の適格性評価 ・既存取引業者 → 過去の取引実績の再評価 |
| 4.書面調査 | 原薬供給業者(製造所、国内管理人)への書面調査 ・GMPの遵守状況 ・規制当局からの査察実績 ・日本への供給実績の確認(海外製造所の場合) ・その他、多岐にわたる原薬及び製造所の管理状況等を調査 |
| 5.実地確認 | 品質評価、書面調査により選抜された良好な製造所の実地確認 ・GMPの遵守状況や製造方法の実地確認を行い採用の最終判断 |
| 6.選定 | 評価結果を社内協議し選定 ・品質面、技術面、供給面、購買面など多角的に評価し選定する |
1.求める原薬要件の明確化
▼この表は横にスクロールできます
| 開発対象品の情報収集 | ・原薬特許、製剤特許、販売数量、その他 |
|---|---|
| 原薬供給業者からの情報収集 | ・原薬の物性、結晶形、粒度、純度、残留溶媒、製造方法、安定性、価格、その他 |
| 社内(開発部門・製造部門) からの情報収集 |
・原薬の購入時期、数量、製剤製造に必要な原薬特性、その他 |
2.品質評価
様々な観点からサンプルの品質評価を行います。
3.原薬供給業者の評価と選定
安定供給、高品質医薬品の製造を維持する為には、情報共有が円滑に行える信頼できる原薬供給業者(製造所、国内管理人)を選定することが重要です。
▼この表は横にスクロールできます
| 供給業者(国内管理人)の選定要件 |
・科学的な知識は勿論、日本の薬事制度の知識を有している。 ・適切な組織体制である。 ・意思疎通がスムーズにできる。 |
|---|
4.書面調査
原薬供給業者(製造所、国内管理人)へ、原薬及び製造所管理状況等についての調査表の記入並びに根拠資料の提供を依頼し、記入内容について評価を行います。
調査する項目としては、
製造所のGMP組織体制、GMPの遵守状況、規制当局からの査察実績、国内での原薬保管場所、品質担保の方法、原薬価格、日本への供給実績の確認(海外製造所の場合)、原薬の結晶形、粒度コントロールの可否、不純物提供の可否、特許見解等

5.実地確認
品質評価、書面調査にて良好と選抜された製造所について、品質部門担当者がGMPの遵守状況や製造方法の実地調査を行い、採用の最終判断を行います。
6.選定
上記1.~6.の評価結果より、総合的に原薬供給業者(製造所、国内管理人)を選定しています。
原薬マルチソース化
自然災害等で原薬供給が不安定になるリスクを回避するため、製造所は勿論、製造国が異なる原薬でのマルチソース化に取り組んでいます。
原薬製造国の公開
日新製薬では、ジェネリック医薬品の一層の信頼を頂けるよう、原薬製造国の公開を行っています。



